Nghiên cứu hành vi tái ôxy hóa thép lỏng
06/12/2017
Bài báo trình bày một số kết quả nghiên cứu hành vi tái ôxy hóa thép lỏng. Thí nghiệm xác định mức độ cháy hao các nguyên tố khi thép lỏng tiếp xúc với môi trường không khí đã được tiến hành trong lò điện cảm ứng trung tần dung tích 10 kg tại Trường Đại học Bách Khoa Hà Nội.
Study on reoxidation behavior of liquid steel
Bùi Anh Hòa, Nguyễn Sơn Lâm Trường Đại học Bách khoa Hà Nội
Tóm tắt
Các kết quả về sự cháy hao các nguyên tố (C, Si, Mn, Al), phân bố tạp chất phi kim cho thấy ảnh hưởng của vấn đề tái ôxy hóa thép lỏng đến chất lượng thép là không thể bỏ qua và cần phải được nghiên cứu một cách hệ thống.
Abstract
In this paper the reoxidation behavior of liquid steel is presented. In order to determine loss of the elements (C, Si, Mn, Al) due to reoxidation, experiments of exposing liquid steel in the atmosphere have been conducted using a medium-frequency induction furnace with 10 kg capacity at the Hanoi University of Technology (HUT). Reduction of alloying element content and non-metallic inclusions distribution showed that the influence of liquid steel reoxi- dation on the steel quality is significant and must be investigated systematically.
1. Đặt vấn đề
Thực tế và lý thuyết đã chứng minh rằng độ sạch của thép càng cao thì tính năng và cơ tính của thép càng tốt, tuổi thọ sử dụng càng cao, mang lại hiệu quả kinh tế cao [1,2]. Để sản xuất thép sạch, trước hết phải biết các yêu cầu về tính năng của thép cần sử dụng, sau đó là xá định các khiếm khuyết trong quá trình sản xuất; như vậy mới có thể khống chế chúng trong từng khâu của quá trình sản xuất. Khi hội nhập toàn cầu hóa, chúng ta không thể không nghiên cứu công nghệ sản xuất thép sạch để, nâng cao dần chất lượng thép hiện đang sản xuất ở các nhà máy trong nước. Rõ ràng, việc sản xuất thép có chất lượng cao là mục tiêu phấn đấu của các cơ sở sản xuất trong nước, để đáp ứng nhu cầu thị trường, do đó đã đến lúc phải quan tâm tới vấn đề chống tái ôxy hóa thép lỏng. Chất lượng thép hiện nay không thể nâng cao, mặc dù chúng đã được tinh luyện (trong lò hoặc ngoài lò) và làm sạch, vì các tạp chất mới hình thành phần lớn vẫn nằm lại trong sản phẩm thép [3,4]. Chỉ có quan tâm tới toàn bộ quá trình sản xuất thép mới nâng cao được chất lượng thép và hiệu quả kinh tế trong sản xuất.
Tái ôxy hóa (hay còn gọi là ôxy hóa lần hai) được định nghĩa là sự tăng tổng hàm lượng ôxy trong thép lỏng do phản ứng của sắt (Fe) và các nguyên tố hợp kim khác (Mn, Si, Al, ...) với ôxy trong không khí hoặc với các ôxyt từ xỉ hoặc từ các chất khác bị dòng thép cuốn vào. Tái ôxy hóa không những làm giảm chất lượng của phôi thép mà còn làm cháy hao các nguyên tố hợp kim trong thép, đặc biệt là các nguyên tố hợp kim vi lượng (V, Ti, B, ...) có giá thành cao và có ái lực hóa học mạnh với ôxy. Việc cháy hao các nguyên tố hợp kim làm giảm các tính chất của thép, đồng thời làm giảm hiệu suất thu hồi các nguyên tố hợp kim này. Ngoài ra, hiện tượng tái ôxy thép lỏng còn là nguyên nhân chủ yếu gây nên tắc miệng rót thùng trung gian trong quá trình đúc liên tục [5].
Bài báo này đề cập đến một trong những nguyên nhân gây ra tái ôxy hóa, đó là khi bề mặt thép lỏng tiếp xúc trực tiếp với không khí. Các kết quả thí nghiệm được phân tích và đánh giá nhằm làm sáng tỏ nội dung trên.
2. Thực nghiệm
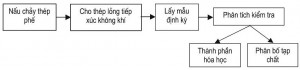
Các thí nghiệm được thực hiện tại Phòng thí nghiệm Công nghệ luyện kim, Bộ môn Kỹ thuật gang thép, nhằm nghiên cứu sự giảm hàm lượng các nguyên tố có ái lực hóa học với ôxy khi có sự tiếp xúc giữa bề mặt thép lỏng và không khí xung quanh, tức là sự cháy hao các nguyên tố do hiện tượng tái ôxy hóa thép lỏng. Các số liệu được phân tích và kiểm tra trên các thiết bị của trường Đại học Bách khoa Hà Nội và một số đơn vị khác. Lò điện cảm ứng trung tần dung tích 10 kg được sử dụng để nấu luyện thép, các mẫu thép được lấy theo từng điều kiện nghiên cứu cụ thể, và sau đó được phân tích thành phần hóa học. Một số mẫu thép trước và sau khi bị tái ôxy hóa được kiểm tra bằng kính hiển vi quang học sự khác nhau về hình thái và sự phân bố của tạp chất. Quy trình thí nghiệm được tiến hành theo sơ đồ trong hình 1.
Hình 1. Sơ đồ quy trình thí nghiệm
3. Kết quả và thảo luận
3.1. Mức độ cháy hao các nguyên tố khi thép lỏng tiếp xúc với không khí
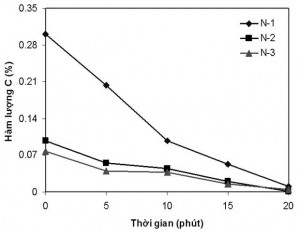
Sau khi nấu chảy thép phế (loại có C trung bình và thấp) trong lò điện cảm ứng trung tần dung tích 10 kg, tiến hành khử ôxy bằng Al, vớt sạch xỉ che phủ trên bề mặt thép lỏng trong lò, rồi lấy mẫu lần thứ nhất. Duy trì công suất điện rất nhỏ, giữ thép lỏng tiếp xúc với không khí trên bề mặt ở nhiệt độ 1600°C, lấy mẫu định kỳ theo thời gian. Nhiệt độ thép lỏng được xác định bằng hỏa quang kế kỹ thuật số do Trung Quốc sản xuất. Thành phần hóa học của các mẫu thép được phân tích trên máy quang phổ phát xạ. Kết quả sự giảm hàm lượng C theo thời gian bề mặt thép lỏng tiếp xúc với không khí xung quanh được nêu trong bảng 1 và biểu diễn trong hình 2.
Hình 2. Sự giảm hàm lượng C theo thời gian thép lỏng tiếp xúc với không khí.
| Mẫu TN | Thời gian (phút) | ||||
| 0 | 5 | 10 | 15 | 20 | |
| N-1 N-2 N-3 | 0,301 0,098 0,077 | 0,203 0,055 0,040 | 0,098 0,045 0,038 | 0,053 0,020 0,015 | 0,010 0,001 0,005 |
Bảng 1. Hàm lượng C(%) giảm theo thời gian thép lỏng tiếp xúc với không khí
Kết quả phân tích cho thấy trong cùng điều kiện thí nghiệm, hàm lượng C ban đầu có trong thép lỏng càng lớn thì tốc độ cháy hao của nó khi thép lỏng tiếp xúc với không khí càng lớn. Điều này hoàn toàn phù hợp với nguyên lý chung của nhiệt động học các phản ứng [6]. Như vậy, mối quan hệ giữa Co (hàm lượng C có trong thép lỏng ban đầu) và Ct (hàm lượng C trong thép lỏng sau thời gian t phút) có thể biểu diễn qua công thức (1):
![]()
trong đó k là hệ số (1/phút). Từ công thức (1), chúng ta có công thức (2):
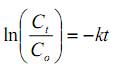
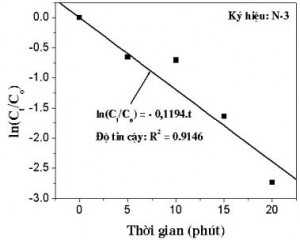
Dựa vào đồ thị biểu diễn mối quan hệ ln(Ct/Co) và thời gian trong hình 3, sử dụng phương pháp bình phương nhỏ nhất, xác định được hệ số k = 0,1194 đối với mẫu thí nghiệm số N-3. Tương tự, hệ số k của các mẫu thí nghiệm số N-1 và N-2 được xác định tương ứng là 0,1431 và 0,1683.
Hình 3. Mối quan hệ ln(Ct/Co) và thời gian
Khi điều kiện thí nghiệm không thay đổi, chờ đợi sẽ nhận được các giá trị k xấp xỉ nhau. Kết quả tính k khác nhau (mặc dù không nhiều) cho thấy C không chỉ cháy hao bởi không khí trên bề mặt thép lỏng, mà còn do vật liệu chịu lửa của áo lò, của xỉ lẫn. Ngoài ra, thành phần hóa học của thép lỏng cũng là yếu tố quan trọng quyết định tới lượng ôxy hòa tan và có ảnh hưởng lớn tới sự tái ôxy hóa của các nguyên tố.
Kết quả sự cháy hao các nguyên tố Al, Si, và Mn trong thép lỏng của một số mẫu thí nghiệm nêu trong bảng 2. Trong thời gian ngắn, mặc dù diện tích tiếp xúc của bề mặt thép lỏng với môi trường không khí không lớn song hàm lượng của chúng giảm mạnh, đặc biệt là Al. Nhận thấy rằng khi hàm lượng các nguyên tố càng lớn thì mức độ cháy hao do tái ôxy hóa càng nhiều, nguyên tố có ái lực hóa học với ôxy càng mạnh thì mức độ cháy hao do tái ôxy hóa càng lớn. Trong thực tế luyện thép, ngoài Al cần phải kể đến Ti, V, Mo,... cũng có ái lực rất mạnh với ôxy. Do vậy, mức độ cháy hao của chúng trong quá trình tái ôxy hóa chắc chắn sẽ không nhỏ, tác hại gây ra đối với sản phẩm càng nhiều. Hơn nữa, việc khống chế chính xác thành phần sẽ gặp khó khăn, công nghệ sản xuất bao gồm nấu luyện, ra thép, và đúc thỏi càng phức tạp. Trong thực tế, diện tích tiếp xúc giữa thép lỏng và không khí rất lớn, thời gian đúc rót dài, nên quá trình tái ôxy hóa thép lỏng xảy ra còn mạnh hơn nhiều so với điều kiện thí nghiệm này.
Nghiên cứu kỹ tỷ lệ cháy hao các nguyên tố trong bảng 2, thấy rằng mẫu thí nghiệm số N-4 có tỷ lệ cháy hao Mn và Si nhỏ hơn nhiều so với mẫu thí nghiệm số N-3. Điều này có thể giải thích bởi thí nghiệm số N-4 có hàm lượng Mn và Si lớn hơn rất nhiều so với thí nghiệm số N-3, và thời gian lấy mẫu của hai thí nghiệm cũng khác nhau. Tuy nhiên, nếu so sánh tương đối lượng cháy hao sẽ thấy không có sự khác biệt nhiều, ví dụ ΔCMn là 0,1588% đối với thí nghiệm N-3 và 0,1839% đối với thí nghiệm N-4.
| Mẫu TN | Lượng nguyên tố (%) | Al | Si | Mn |
| N-3 | Ban đầu | 0,1062 | 0,0267 | 0,2811 |
| Sau 10 phút | 0,0026 | 0,0004 | 0,2033 | |
| Sau 20 phút | 0,0009 | 0 | 0,1223 | |
| Cháy hao | 0,1053 | 0,0267 | 0,1588 | |
| Tỷ lệ (%) | 99,15 | 100 | 56,49 | |
| N-4 | Ban đầu | 0,0999 | 0,1391 | 1,9763 |
| Sau 5 phút | 0,0197 | 0,1305 | 1,7924 | |
| Cháy hao | 0,0802 | 0,0086 | 0,1839 | |
| Tỷ lệ (%) | 80,27 | 6,18 | 4,71 |
Bảng 2. Cháy hao một số nguyên tố khi thép lỏng tiếp xúc với không khí
Tái ôxy hóa thép lỏng chính là sự cân bằng được thiết lập trở lại giữa nguyên tố hòa tan trong thép lỏng với ôxy trong không khí và tạp chất ôxyt tạo thành. ôxy trong không khí có thể liên tục hòa tan vào trong thép lỏng và phản ứng ôxy hóa xảy ra cho đến khi ngừng thí nghiệm hoặc cho đến khi cháy hết các nguyên tố. Khi không khí cuốn vào trong thép lỏng thì xảy ra quá trình hòa tan ôxy vào thép lỏng qua những giai đoạn sau:
- Các phân tử ôxy tiếp xúc với bề mặt thép lỏng và chúng bị phân ly thành các nguyên tử:
1/2{O2} ↔ (O)
- Các nguyên tử ôxy hòa tan vào thép lỏng:
(O) ↔ [O]
- Nguyên tử khí khuếch tán sâu vào trong thép lỏng, tương tác hóa học với các nguyên tố tạo thành hợp chất ôxyt.
Khi ôxy thâm nhập vào trong thép lỏng, các ôxyt được hình thành từ các phản ứng:
[Mn] + [O] = (MnO) ΔGoT = - 288,1 + 0,1283T (kJ/mol) [Si] + 2[O] = (SiO2) ΔGoT = - 581,9 + 0,2218T (kJ/mol) 2[Al] + 3[O] = (Al2O3) ΔGoT = - 1202 + 0,3863T (kJ/mol)
Khi trong thép lỏng có chứa các ôxyt chưa kịp nổi lên hoặc có nguồn gốc từ xỉ hoặc vật liệu chịu lửa thì tùy thuộc vào điều kiện cụ thể sẽ xảy ra các phản ứng [7]:
2(MnO) + [Si] = (SiO2) + 2[Mn] ΔGoT = - 5,7 - 0,0348T (kJ/mol) 2/3(Al2O3) + [Si] = (SiO2) + 4/3[Al] ΔGoT = 0,2194 - 0,0357T (kJ/mol)
Đồng thời, các ôxyt mới tạo thành cũng có thể kết hợp với nhau tạo thành những đám tạp chất ôxyt có nhiệt độ chảy cao (3Al2O3.2SiO2, MnO.Al2O3,...). Phản ứng hoàn nguyên SiO2 bằng Mn có thể xảy ra như sau:
2[Mn] + 3(SiO2) = 2(MnO) + [Si] ΔGoT = - 26,87 - 0,0114T (kJ/mol) (SiO2) + (MnO) = (MnO.SiO2)
Trong trường hợp này, hợp chất (MnO.SiO2) có nhiệt độ chảy thấp, tỷ trọng nhỏ nên dễ tách khỏi thép lỏng hơn các hợp chất ôxyt khác [2]. (SiO2) cũng có thể bị [Al] hoàn nguyên tạo thành (Al2O3), sau đó (Al2O3) lại kết hợp với (CaO) trong xỉ cuốn vào và hình thành từng cụm tạp chất CaO.nAl2O3 chứa nhiều Al2O3.
Để củng cố những nhận định trên, cần tiến hành nghiên cứu hình thái và phân bố tạp chất phi kim trong thép trước và sau khi tái ôxy hóa.
3.2. Sự phân bố tạp chất phi kim
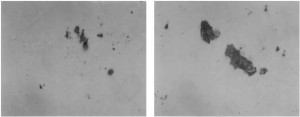
Các mẫu thép được mài nhẵn, đánh bóng, và kiểm tra bằng kính hiển vi quang học với độ phóng đại 100 và 400 để quan sát hình thái với sự phân bố tạp chất phi kim (xem hình 4).
Hình 4. Tạp chất trong mẫu thép (a) trước và (b) sau khi tái oxy hóa (x 400).
Thấy rằng các tạp chất trong mẫu thép bị tái ôxy hóa có kích thước lớn (tới 80 μm, hình 4b), còn tạp chất trong mẫu thép ban đầu chủ yếu là sản phẩm khử ôxy có kích thước nhỏ hơn (trung bình là 20 μm, hình 4a). Như đã nêu ở trên, các tạp chất trong mẫu thép bị tái ôxy hóa thấy phân bố không đều, có xu hướng tập trung, và có thể là những tạp chất ôxyt đa cấu tử. Tùy thuộc vào mức độ ôxy hóa các nguyên tố, tạp chất tái ôxy hóa có thành phần khác nhau. Ngoài các tạp chất ôxyt do tái ôxy hóa các nguyên tố, còn những tạp chất ôxyt khác có nguồn gốc từ vật liệu chịu lửa của áo lò hoặc từ xỉ lẫn vào.
Đặc trưng phân bố tạp chất phi kim như thế, chắc chắn có ảnh hưởng xấu tới chất lượng của sản phẩm thép. Khi cán phôi thép đến kích thước nào đó, các tạp chất này lộ ra bề mặt và là nguyên nhân chính làm xấu chất lượng bề mặt sản phẩm, thậm chí có thể là nguyên nhân gây đứt trong quá trình cán xuống kích thước nhỏ.
4. Kết luận
- Hiện tượng tái ôxy hóa các nguyên tố xảy ra khi có sự tiếp xúc giữa thép lỏng và môi trường không khí - nguồn cung cấp ôxy chủ yếu cho tái ôxy hóa.
- Mức độ tái ôxy hóa các nguyên tố phụ thuộc vào hàm lượng của chúng có trong thép lỏng và ái lực hóa học của chúng với ôxy. - Tạp chất phi kim trong mẫu thép bị tái ôxy hóa chứa cả các tạp chất có kích thước lớn, phân bố không đồng đều nên chắc chắn có ảnh hưởng xấu tới chất lượng của thép. -
Các kết quả thí nghiệm đã khẳng định thêm rằng mặ dù ôxy đã được khử bỏ khỏi thép lỏng, nhưng khi đúc rót thì môi trường không khí, vật liệu chịu lửa, xỉ lẫn,… là nguồn cung cấp ôxy chủ yếu cho phản ứng ôxy hóa các nguyên tố trong thép lỏng.
Vì vậy để nâng cao chất lượng thép cần một nghiên cứu toàn diện hơn về cơ chế tái ôxy hóa, ảnh hưởng của nó tới chất lượng sản phẩm và các biện pháp khắc phục.
[symple_box color="gray" text_align="left" width="100%" float="none"]
Tài liệu trích dẫn
- R. Viswanathan, Application of clean steel and superclean steel technology in the electric power industry, Overview of EPRI research and products; Conference proceedings 6 - 7th March 1995, (London, UK), pp. 1- 32
- Bùi Văn Mưu, Bùi Thanh Bình, ứng dụng silicômangan (SiMn) để khử ôxy trong luyện thép; Tạp chí Khoa học và công nghệ kim loại, Số 11 (tháng 4/2007), trang 26-29
- Hiroki goto and Ken-ichi Miyazawa, Reoxidation behavior of molten steel in non-killed and Al-killed steels; ISIJ international, Vol. 38, No. 3, 1998, pp. 256-259
- Ngô Trí Phúc, Nguyễn Sơn Lâm, Thiết bị và công nghệ đúc phôi thép; Nhà xuất bản Bách Khoa Hà Nội, 2006.
- Katsuhiro Sasai and Yoshimasa Mizukami, Mechanism of alumina adhesion to continuous caster nozzle with reoxidation of molten steel; ISIJ international, Vol. 41, No. 11, 2001, pp. 1331-1339
- Bùi Văn Mưu, Nguyễn Văn Hiền, Nguyễn Kế Bính, Trương Ngọc Thận, Lý thuyết các quá trình luyện kim, Nhà xuất bản Khoa học và kỹ thuật, 2006
- Dong-Chul Park, In-Ho Jung, Peter C. H. Rhee and Hae-Geon Lee, Reoxidation of Al-Ti containing steels by CaO-Al2O3-MgO-SiO2 slag; ISIJ International, Vol. 44, No. 10, 2004, pp. 1669-1678.
[/symple_box][symple_clear_floats]