Hoàn thiện công nghệ xử lý tổng hợp bùn dương cực trong quá trình điện phân thiếc tinh 99,95% để thu các nguyên tố có ích: Sn, Cu, As, Bi, Au... ở quy mô mở rộng
06/12/2017
Trong quá trình sản xuất thiếc bằng phương pháp điện phân sẽ sinh ra bùn dương cực, hàm lượng thiếc trong bùn dương cực rất cao và các nguyên tố đi cùng... hàm lượng tuy không lớn nhưng lại có giá trị cao về mặt kinh tế. Vì vậy việc xử lý để thu hồi chúng là rất cần thiết.
Improved processing anode mud during Sn electrolysis for recovery of useful elements Sn, Cu, As, Bi, Au...
Nguyễn Văn Chiến và Trần Văn Vụ Viện Khoa học và Công nghệ Mỏ - Luyện kim
Tóm tắt
Trong quá trình sản xuất thiếc loại I để phục vụ xuất khẩu bằng phương pháp điện phân sẽ sinh ra bùn dương cực, hàm lượng thiếc trong bùn dương cực rất cao, còn các nguyên tố đi cùng (Cu, As, Bi, Au …) hàm lượng tuy không lớn nhưng lại có giá trị kinh tế cao. Vì vậy việc xử lý thu hồi chúng là cần thiết. Trong bài viết giới thiệu kết quả nghiên cứu các điều kiện tối ưu để tách các nguyên tố có ích từ bùn dương cực, các chỉ tiêu kinh tế của quá trình công nghệ và lưu trình công nghệ thích hợp.
Abstract
During production process of the 1st type tin (99,95%Sn) - one of exported products, an anode mud of high Sn content containning useful elements such as Cu, As, Bi, Au,... is formed thus the recovery of this anode mud is necessary. In this paper the optimal technological and economic conditions of the process, separating these elements from anode mud, are presented.
1. Mở đầu
Việc sản xuất thiếc 99,95% có hàm lượng chì thấp (< 0,005% ) rất phù hợp với nhu cầu sản xuất đồ hộp và nâng giá thành sản phẩm thiếc. Trong quá trình sản xuất thiếc bằng phương pháp điện phân sẽ sinh ra bùn dương cực, tuy bùn dương cực chỉ chiếm khoảng 1% đến 5% (tùy thuộc độ sạch của thiếc) nhưng hàm lượng thiếc trong bùn dương cực rất cao và các nguyên tố đi cùng (Cu, As, Bi, Au ...) hàm lượng tuy không lớn nhưng lại có giá trị cao về mặt kinh tế. Vì vậy việc xử lý để thu hồi chúng là rất cần thiết.
Mục tiêu nghiên cứu là:
1- Thiết lập các điều kiện tối ưu để tách các nguyên tố có ích từ bùn dương cực (thiếc, đồng, vàng, bitmut...).
2- Xác định các chỉ tiêu kỹ thuật của quá trình công nghệ.
3- Xây dựng được lưu trình công nghệ thích hợp để thu hồi thiếc và các nguyên tố có ích ở quy mô mở rộng.
2. Thực nghiệm
Các nguyên tố trong bùn dương cực tồn tại chủ yếu ở dạng kim loại. Để tách các nguyên tố này thông thường người ta thiêu ôxy hóa trong lò có nhiệt độ tối đa 1000°C. Các phản ứng xảy ra trong quá trình nung :
Sn + O2 = SnO2 4Bi + 3O2 = 2Bi2O3 2Cu + O2 = 2CuO 4Fe + 3O2 = 2Fe2O3 4As + 3O2 = 2As2O3
Các kim loại, các hợp chất của các nguyên tố cần thu hồi chủ yếu nằm trong bùn dương cực, riêng asen và antimon trong điều kiện thích hợp dễ bay hơi phần lớn, vì vậy có thể tách chúng bằng cách thiêu. Dựa vào độ hòa tan của ôxyt các kim loại còn lại rất khác nhau trong axit, sẽ hòa tách chúng trong môi trường axit có nồng độ khác nhau.
Ôxyt đồng dễ dàng hòa tan trong axit sunphuric loãng theo phản ứng:
CuO+ H2SO4 = CuSO4 + H2O
Bitmút và chì cũng như asen và antimon còn lại được hòa tan trong axit clohyđric theo phản ứng:
Me2Ox + 2xHCl = 2MeClx + x H2O
Bitmút được tách khỏi dung dịch bằng phương pháp thủy phân.
BiCl3 + H2O = BiOCl + 2HCl
Trong đề tài này chúng tôi tiến hành nghiên cứu hòa tách các nguyên tố chứa trong bùn dương cực ra khỏi thiếc bằng axit, sau đó hòa tách vàng bằng phương pháp xyanua.
Tùy thuộc chất lượng thiếc đưa vào điện phân mà hàm lượng các nguyên tố có trong bùn khác nhau. Theo kết quả phân tích, bùn dương cực điện phân tại xưởng Tam Hiệp - Viện Nghiên cứu Mỏ và Luyện kim có hàm lượng như bảng 1.
| Hàm lượng, % | Hàm lượng, g/t | |||||||
| Sn | Cu | Bi | As | Sb | Pb | Fe | Au | Ag |
| 49-50 | 7-10 | 7-10 | 3-4 | 2-3 | 5-8 | 3-4 | 50-90 | 350 |
Bảng 1. Hàm lượng các nguyên tố trong bùn dương cực
Nhìn từ bảng 1 thấy đồng, bítmút có hàm lượng tương đối lớn, vàng với hàm lượng tuy nhỏ nhưng xét về mặt kinh tế lại có giá trị cao.
Đồng sau khi tách có thể chuyển thành kim loại sẽ được sử dụng nhiều trong thực tế, hoặc chuyển thành muối sunphát đồng cũng rất có giá trị. Bitmút có thể chuyển thành bitmút ôxyclorua dùng trong hóa mỹ phẩm rất tốt. Vàng là kim loại quý.
Để hiệu suất thu hồi thiếc cao phải tiến hành thiêu sao cho thiếc chuyển hoàn toàn về dạng ôxyt thiếc.
Ôxyt các kim loại (trừ thiếc) có thể tan trong axit, vì vậy có thể tách nó ra khỏi ôxyt thiếc.
Kết quả quá trình thiêu phụ thuộc vào thời gian và nhiệt độ, độ xốp của mẫu.
Quá trình thiêu mẫu tiến hành chia làm ba giai đoạn
Giai đoạn 1: Đưa nhiệt độ lớp liệu lên đến 4000C, giữ ở nhiệt độ này 4 giờ, mục đích sấy khô bùn và tránh bùn bị vón cục.
Giai đoạn 2: Đưa nhiệt độ lớp liệu lên 6000C, giữ ở nhiệt độ này trong khoảng 4 giờ. Giai đoạn này ôxy hóa gần như toàn bộ các cấu tử trong liệu.
Giai đoạn 3: Đưa nhiệt độ lên 9000C, giữ ở nhiệt độ này trong thời gian 4 giờ. Giai đoạn này vừa để ôxy hóa toàn bộ các kim loại vừa để bốc hơi asen và antimon.
Để tăng cường sự khuếch tán của ôxy vào lớp liệu cần phải thường xuyên cào đảo và có quạt hút sao cho không khí thường xuyên tiếp xúc với lớp liệu, quá trình ôxy hóa sẽ hoàn thiện hơn.
Mẫu sau khi sấy khô, tiến hành thiêu theo ba giai đoạn như trên, kết quả nhận được nêu ra ở bảng 2.
| Hàm lượng, % | Hàm lượng, g/t | |||||||
| Sn | Pb | Cu | Fe | As | Sb | Bi | Au | Ag |
| 52,5 | 7,9 | 10,3 | 3,5 | 0,5 | 0,4 | 9,5 | 75,5 | 365 |
Bảng 2: Hàm lượng các nguyên tố trong mẫu sau khi thiêu
Nhìn vào bảng 2 chúng ta thấy asen và antimon hao đi khá nhiều, thiếc kim loại kiểm tra bằng cách hòa tan bùn sau khi thiêu với axit clohyđric không có. Điều đó chứng tỏ tiến hành thiêu như thế thiếc đã chuyển hoàn toàn thành ôxyt thiếc.
3. Kết quả
3.1. Quá trình tách đồng
Bùn sau khi thiêu tác dụng với axit sunphuric, có thể xảy ra phản ứng sau:
Me2Oy + yH2SO4 = Me2(SO4)y + yH2O
Dựa vào tính chất hóa học của ôxyt đồng dễ tan trong axit hơn các ôxyt các kim loại khác chứa trong bùn nên có thể nghiên cứu tách đồng khỏi bùn bằng dung dịch axit sunphuric loãng. Quá trình hòa tách ôxyt đồng phụ thuộc vào nhiệt độ, nồng độ axit sunphuric, thời gian hòa tách, tỷ lệ rắn lỏng đồng, còn ôxyt các kim loại khác hầu như không tan trừ sắt. Sau khi hòa tan phải tách sunphát sắt khỏi sunphát đồng.
CuO+ H2SO4 = CuSO4 + H2O FeO+ H2SO4 = FeSO4 + H2O
Làm sạch đồng sunphát bằng Cu(OH)2. Quá trình xảy ra như sau:
2Fe2(SO4)3 + 6Cu(OH)2 = 4Fe(OH)3 + 6CuSO4
Qua nghiên cứu, đã chọn:
- Tỷ lệ rắn/lỏng : 1/3. - Lượng axit gấp 1,5 đến 2 lần đồng theo phản ứng. - Thời gian hòa tách: (4 - 5)h. - Dung dịch sunphat đồng thu được cô đặc đến kết tinh sunphát đồng thô. Sunphát đồng thô kết tinh lại thu được sunphát đồng sạch.
3.2. Khả năng tách các ôxyt của các kim loại còn lại khỏi ôxyt thiếc
Ôxyt thiếc rất khó tan trong các axit, kể cả axit đặc nóng. Do đó, có thể dễ dàng làm sạch ôxyt thiếc bằng axit clohydric.
Quá trình hòa tách chia làm bốn bước:
Bước 1: Hòa tách bằng axit clohyđric 1:3 trong thời gian 4 giờ.
Giai đoạn này ôxyt các kim loại có trong bùn như đồng, chì, sắt, asen, antimon, bítmút cơ bản chuyển hóa thành muối clorua tan trong nước, trừ chì. Vì chì clorua là hợp chất ít tan. Bùn còn lại chủ yếu là SnO2, Au, Ag.
Bước 2: Lọc giữ dung dịch trong (dung dịch 1 ).
Bước 3: Rửa liệu bằng dung dịch axit clohyđric 1 : 7.
Bước 4: Rửa liệu bằng nước sạch (cặn 1) . Sau giai đoạn này lấy sản phẩm, chuyển vào lò luyện thiếc thô. Đã sử dụng cặn 1 làm nguyên liệu để nghiên cứu hòa tách vàng bằng phương pháp xianua.
3.3. Quá trình tách bitmut
Dung dịch trong (dung dịch 1) sau khi hòa tách bằng axit clohyđric, bitmut nằm ở dạng Bi 3+ trong dung dịch, để tách bitmut khỏi dung dịch này, tiến hành thủy phân bitmut theo phản ứng:
Bi 3++ H2O + 3 Cl - = BiOCl + 2 HCl
Đã áp dụng phương pháp thủy phân bitmut từ dung dịch 1 bằng cách điều chỉnh nồng độ HCl xuống còn 20g/l bằng NaOH, có mặt của H2O2. Lọc rửa kết tủa bằng dung dịch axit clohydric 1/7, thu được BiOCl thô. Hoà tan BiOCl thô bằng axit clohyđric để tinh chế lại, thu được sản phẩm 2. Kết quả nghiên cứu thể hiện trên bảng 3.
| Sản phẩm | Thành phần, % | ||||||
| Bi | Sb | As | Fe | Cu | Pb | BiOCl | |
| Trước tinh chế | 72,3 | 0,8 | 1,2 | 0,2 | 0,05 | 0,01 | 90,1 |
| Sau tinh chế (SP 2) | 79,2 | 0,012 | 0,005 | 0,021 | 0,003 | - | 98,5 |
Bảng 3: Các chỉ tiêu đạt được sau thủy phân
3.4. Thu hồi vàng
Quá trình trình thu hồi vàng bằng phương pháp xianua. Tuy rất nhiều kim loại có thể hòa tan cùng vàng trong dung dịch chứa CN- để tạo phức với vàng, nhưng trong mẫu này đã hòa tách chủ yếu ra khỏi mẫu nghiên cứu (cặn 1). Vì vậy quá trình nghiên cứu thu hồi vàng không gặp nhiều cản trở. ở đây chỉ chú ý đến sự phụ thuộc của nồng độ CN- , cũng như tỷ lệ rắn lỏng và chất ôxy hóa đến quá trình hòa tách vàng.
Qua nghiên cứu, đã rút ra được các thông số tối ưu để thu hồi vàng từ bùn dương cực:
- Lượng NaCN : 3g/kg bùn dương cực. - Thời gian hòa tách: 48 h. - Thời gian hoàn nguyên: 48 h. - Lượng kẽm hoàn nguyên: 4 đến 5 g/1kg bùn.
Trong quá trình thu hồi vàng, thu hồi được cả bạc kim loại, tuy nhiên lượng bạc không lớn.
Thu hồi ôxyt thiếc: Bã sau khi hòa tách vàng, rửa sạch, sấy khô thu được ôxyt thiếc để sản xuất thiếc thô (sản phẩm 4).
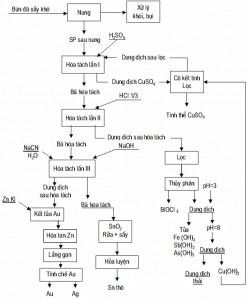
Sau quá trình nghiên cứu, đã đưa ra lưu trình công nghệ xử lý bùn dương cực (hình 1).
Hình 1. Sơ đồ công nghệ xử lý bùn dương cực
3.5. Sản xuất thử
Sau khi đưa ra lưu trình công nghệ xử lý bùn dương cực, đã tiến hành xử lí mẫu bùn trên với lượng bùn khô 100 kg.
| TT | Kim loại hòa tách | Hàm lượng (%) | Thu hồi | Hiệu suất (%) | Ghi chú | |
| Khối lượng SP (kg, g) | Hàm lượng SP (%) | |||||
| 1 | Sn | 49,5 | 70,1 | 68,5 | 97,00 | |
| 2 | Cu | 9,5 | 296,4 | 25,2 | 78,62 | Sản phẩm còn ở dd |
| 3 | Bi | 8,9 | 99,6 | 98 | 90 | |
| 4 | Au | 70 g/t | 6,37 | 99 | 90,09 | |
Bảng 4. Bảng tổng hợp kết quả thu hồi các sản phẩm
Chuyển 100 kg bùn dương cực vào lò thiêu theo chế độ đã nghiên cứu. Sau đó chuyển vào bình hòa tách, thêm 400 lít dung dịch axit sunphuric có nồng độ đã nghiên cứu, khuấy đều trong thời gian 4h, để lắng, lọc lấy dung dịch trong (dung dịch 1). Rửa cặn bằng nước đến sạch H2SO4, thêm 300 lít dung dịch HCl 1/3, khuấy đều (4 - 5) h.
Để lắng, lọc gạn, giữ dung dịch (dung dịch 2). Tiếp tục hai lần nữa (dung dịch hòa tách lần hai có thể nhập vào dung dịch 2). Dung dịch hòa tách lần ba có thể bỏ đi. Rửa cặn ba lần bằng nước nóng, rửa tiếp hai lần bằng nước lạnh. Thêm 300 lít nước, điều chỉnh pH bằng 9. Thêm 300 g NaCN. Khuấy đều 48h, có mặt oxy. Để lắng lọc gạn lấy dung dịch trong (dung dịch 3).
Thêm 100 lít nước, khuấy đều, lọc gạn nhập dung dịch vào dung dịch 3. Rửa tiếp cặn bằng nước và giữ dung dịch cho mẻ sau. Thêm vào dung dịch 3 khoảng 1,5 kg kẽm kim loại, khuấy nhẹ, sau 48h lấy tủa xử lý thu hồi vàng sản phẩm 3. Phần cặn phơi khô thu được sản phẩm 4. Dung dịch 2 điều chỉnh nồng độ HCl đến nồng độ 20g/l.
Để lắng, lọc lấy kết tủa đem thủy phân lại được sản phẩm (sản phẩm 2). Dung dịch điều chỉnh pH bằng 4, lọc bỏ cặn, phần dung dịch trong diều chỉnh pH bằng 8, lọc lấy kết tủa chuyển vào dung dịch 1. Dung dịch 1 cô kết tinh CuSO4, CuSO4 kết tinh lại được sản phẩm 1.
4. KẾT LUẬN
Đã thiết lập được quy trình công nghệ có các thông số kỹ thuật đảm bảo tách riêng rẽ và thu hồi các nguyên tố có trong bùn dương cực ở qui mô phòng thí nghiệm và qui mô mở rộng tại xưởng điện phân.
Các sản phẩm có ích được thu hồi là:
- SnO2: hàm lượng (68 - 69)%, thực thu 97%. - CuSO4.5H2O: 98%, thực thu 93%. - BiOCl: 99%, thực thu tính theo Bi 90%. - Au : 98%, thực thu 90%. - As: định hướng xử lý môi trường.