Cơ chế phản ứng nhiệt cacbon của TiO2 khi sử dụng nghiền năng lượng cao
06/12/2017
Bài báo này trình bày nghiên cứu sử dụng phương pháp nghiền năng lượng cao tác động đến cơ chế tổng hợp TiC nhằm giảm nhiệt độ tổng hợp và giảm giá thành TiC.
The mechanism of carbothermal reduction process of TiO2 using high-energy mechanical milling
Vũ Huy Thăng Bộ Giáo dục và Đào tạo, Email: Thangkhh@gmail.com Trần Quốc Lập Trường Đại học Bách khoa Hà Nội
Ngày nhận bài: 15/8/2014, Ngày duyệt đăng: 22/8/2014
TÓM TẮTSử dụng nghiền năng lượng cao để tổng hợp cacbit titan (TiC) từ đioxit titan (TiOOO2) và muội than (C) đã được thực hiện trong nghiên cứu này. Kết quả phân tích nhiễu xạ rơnghen và phân tích nhiệt (DTA) của những mẫu nghiền với thời gian khác nhau cho, thấy nghiền năng lượng cao đã thúc đẩy phản ứng tổng hợp TiC. Trong giai đoạn liên quan đến quá trình tạo tiền chất của TiC, khối lượng mất đi trong hỗn hợp bột tăng từ 25,26 % đến 38,43 % tương ứng với thời gian nghiền tăng từ 6 giờ đến 30 giờ. Trong phản ứng tạo TiC từ các tiền chất, khối lượng bột mất đi tăng từ 38,42 % đến 45,28 % tương ứng với thời gian nghiền tăng từ 6 giờ đến 30 giờ. Hơn nữa, với cùng quá trình thiêu kết, hàm lượng cacbon liên kết trong TiC nhận được đã giảm theo thời gian nghiền.
Từ khóa: Nghiền năng lượng cao, oxit titan hàm lượng thấp, phân tích nhiệt vi sai, tổng hợp TiC, nhiễu xạ rơnghen
ABSTRACTThe high-energy mechanical milling for synthesis of TiC from TiOiO2 and C powders was realized in this work. The analyzing of X-ray diffraction patterns and DTA curves of samples, milled for different times, showed that the high-energy mechanical milling process gave an impulse to the synthesis of TiC. In the stag is connected with the formation of the precursor of TiC, the mass lose in the mixture increased from 25,26% to 38.43% with increasing from 6h to 30h milling time. In the stag is connected with the formation of the precursor of TiC, the mass lose in the mixture increased from 25,26% to 38.43% with increasing from 6h to 30h milling time. In the reaction formed TiC from the precursor, the mass lose increased from 38,42% to 45.28% with increasing from 6h to 30h milling time. Furthermore, in the same sintering process, the bonded carbon content in the formed TiC increased with increas- ing milling time.
Keywords: High-energy milling, lower titanium oxide, DTA, the synthesis of TiC, X-ray diffraction.
1. Đặt vấn đề Cacbit titan (TiC) là hợp chất có cấu trúc mạng kiểu NaCl. TiC có nhiều tính chất nổi trội như độ cứng cao, chịu mài mòn, chịu va đập và là hợp chất khó nóng chảy nên được sử dụng rộng rãi trong nhiều lĩnh vực. Tuy nhiên, tổng hợp TiC đòi hỏi điều kiện khắt khe, thiết bị đặc biệt nên chi phí rất cao. Nhằm giảm bớt giá thành sản phẩm, nên trên 80 % TiC được sản xuất từ TiOiO2 do trong tự nhiên titan tồn tại chủ yếu dưới dạng các oxit [1-5]. Cơ chế tổng hợp TiC từ TiO2 và C đã được nhiều nhà nghiên cứu thừa nhận đề xuất của Meerson và Lipkes [6], là cơ chế 3 giai đoạn [7-9]. Giai đoạn thứ nhất là các phản ứng khử oxy bằng C, kết quả là khí CO bay ra với một loạt các oxit titan có hàm lượng oxy thấp hơn được tạo thành:2TiO2 + C →đ TiO2O3 + CO (1)
Phản ứng (1) xảy ra ở nhiệt độ khoảng 1200ºC [6]. Belyakova cho rằng, hợp chất trung gian TiO2O3 có cấu trúc mạng lập phương là sản phẩm cuối cùng của giai đoạn này. Tuy nhiên, Samsonov cũng như Kutsev và Ormont [6] lại cho rằng, hợp chất trung gian và sản phẩm cuối cùng của giai đoạn này là hợp chất TiO3O5 được tạo ra theo phản ứng:3TiO2 + C →đ TiO3O5 + CO (2)
Theo Y.-C. Woo [9], hợp chất trung gian TiO3O5 là sản phẩm cuối cùng của giai đoạn này và được tạo ra từ TiO4O7, sản phẩm của phản ứng:4TiO2 + C →đ TiO4O7 + CO (3)
Phản ứng (3) xảy ra ở nhiệt độ 1087oC và tạo ra TiO4O7 là tiền chất của TiO3O5:3TiO4O7 + C →đ TiO3O5 + CO (4)
Trong kết quả thực nghiệm của nghiên cứu này, TiO3O5 và TiO2O3 cùng tồn tại ở sản phẩm nghiền năng lượng cao. Tuy nhiên, hợp chất TiO3O5 chiếm chủ yếu trong hỗn hợp, do bột sử dụng để nghiên cứu chủ yếu là TiO2-anataz và một phần nhỏ TiO2-rutil. Có thể nói nguyên nhân ở đây chính là việc sử dụng TiO2-rutil hay TiO2-anataz để tổng hợp TiC. Trong công trình của Luchinsky [4], TiO2-rutil và TiO2- anataz có công thức hóa học là TiO2, nhưng cấu trúc phân tử của TiO2-rutil là Ti2O4 và phân tử TiO2- anataz có cấu trúc Ti4O8, đồng ý với Y.-C. Woo là hợp chất TiO3O5 được tạo ra từ TiO4O7. Quá trình làm giảm hàm lượng oxy của TiO2 là quá trình mất dần từng nguyên tử O của phân tử TiO2. Theo L.-M. Berger [8], cơ chế vận chuyển chất chủ yếu của quá trình là cặp khí (CO và CO2). Đầu tiên CO được sinh ra trong phản ứng trên bề mặt tiếp xúc giữa TiO2 và C, sau đó CO được vận chuyển đến bề mặt hạt oxit titan và trở thành tác nhân làm giảm hàm lượng oxy trong oxit titan để tạo ra CO2. CO2 sinh ra được đưa đến bề mặt hạt bột C và tác dụng với C để tái sinh ra CO theo phản ứng:CO2 + C →đ 2CO (5)
Giai đoạn thứ hai của quá trình là TiCxOy, tiền chất của TiC, được tạo ra từ TiO3O5 và TiO2O3. Theo L.- M. Berger [6], trong giai đoạn này CO là tác nhân chính gây ra phản ứng làm giảm hàm lượng oxy trong oxit titan và tạo ra CO2. Đồng thời với quá trình này là các nguyên tử C xâm nhập vào mạng tinh thể, chiếm vị trí của các nguyên tử O đã mất đi. Hợp chất TiCxOy là sản phẩm cuối cùng của giai đoạn thứ hai. ở đây x+y ≤ 1 do tốc độ thoát ra của các nguyên tử O và tốc độ khuếch tán vào lỗ hổng của các nguyên tử C là không bằng nhau. Sau giai đoạn này, trong mạng tinh thể tiền chất của TiC xuất hiện nhiều khuyết tật [8-9]. Giai đoạn thứ ba của quá trình là phản ứng thế của các nguyên tử C vào vị trí các nguyên tử O trong mạng tinh thể hợp chất TiCxOy. Với mật độ khuyết tật lớn, hàm lượng oxy rất thấp nên chủ yếu ở giai đoạn này là quá trình xâm nhập các nguyên tử C vào mạng tinh thể làm hàm lượng C trong tinh thể tăng lên. Tiếp tục quá trình ở giai đoạn hai, sự thoát ra của các nguyên tử oxy vẫn nhờ cặp khí CO và CO2. Cuối cùng của giai đoạn này là TiC được tạo ra. Bài báo này trình bày nghiên cứu sử dụng phương pháp nghiền năng lượng cao tác động đến cơ chế tổng hợp TiC nhằm giảm nhiệt độ tổng hợp và giảm giá thành TiC. 2. Thực nghiệm Bột TiOiO2-anataz được sử dụng có kích thước khoảng 200 μm và độ sạch trên 99%. Cacbon được sử dụng là muội than có kích thước khoảng 200 μm. Tỷ lệ thành phần về khối lượng hỗn hợp bột được tính theo phản ứng:TiO2 + 3C = TiC + 2CO (6)
Hỗn hợp bột với tỷ lệ về khối lượng TiO2:C là 68:32, được trộn đều và nghiền trong máy nghiền hành tinh Pulverisette 5. Tốc độ nghiền là 350 vòng/phút, tỷ lệ bi:bột là 20:1. Các mẫu cùng thành phần được nghiền với thời gian là: 0, 6, 12, 18, 24 và 30 giờ. Các mẫu được khảo sát trên máy nhiễu xạ rơnghen D8-Advance, với chế độ là 40 kV; 40 mA, bức xạ CuKá có bước sóng λ = 1,5406 và phân tích nhiệt vi sai trên thiết bị Setsys Evolution 24 trong môi trường khí Ar. 3. Kết quả và thảo luận Ảnh hưởng của nghiền năng lượng cao tới cơ chế các phản ứng tổng hợp TiC từ TiOiO2 và C được nghiên cứu bằng các giản đồ nhiễu xạ rơnghen và đường cong phân tích nhiệt (DTA) của những mẫu với thời gian nghiền khác nhau. Hình 1 là đường cong phân tích nhiệt (DTA) và phân tích khối lượng (TG) của hỗn hợp bột TiO2 và muội than sau 6 giờ nghiền. Đường phân tích nhiệt (DTA) chỉ ra rằng, quá trình tổng hợp TiC bắt đầu xảy ra ở nhiệt độ 698ºC và quá trình làm giảm hàm lượng oxy tạo ra TiO3O5 kết thúc ở nhiệt độ 906ºC. Trong các nghiên cứu [6, 10], phản ứng tạo TiO3O5 xảy ra ở nhiệt độ khoảng 1200ºC. Như vậy, đối với các mẫu nghiền năng lượng cao, nhiệt độ tạo TiO3O5 đã giảm xuống, trong Hình 1. Đường cong DTA và TG của mẫu sau 6 giờ nghiền nghiên cứu trước [1], chỉ ra rằng do nghiền năng lượng cao đã bổ sung vào hỗn hợp bột một lượng năng lượng đáng kể được dự trữ trong hạt bột và thúc đẩy quá trình khi thiêu kết. [caption id="attachment_1364" align="aligncenter" width="300"]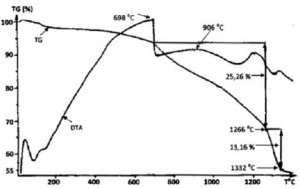 Hình 1. Đường cong DTA và TG của mẫu sau 6 giờ nghiền[/caption]
Hình 1 cho thấy, phản ứng tạo thành TiOxCy bắt đầu từ nhiệt độ 1266ºC và hoàn thành trong 6,5 phút khi nung đến nhiệt độ 1332ºC. Trong nghiên cứu về khử nhiệt cacbon tổng hợp TiC [9], Y.-C.Woo cho rằng, phản ứng tạo thành TiOxCy hoàn thành ở nhiệt độ 1500ºC trong 5 phút trong môi trường khí Ar. Như vậy, so với mẫu không nghiền, nhiệt độ phản ứng tạo TiOxCy cũng giảm xuống đối với mẫu có nghiền năng lượng cao.
Đường cong biến đổi khối lượng (TG) trên hình 1 chỉ ra rằng, lượng khí oxit cacbon thoát ra ở cả hai giai đoạn này làm khối lượng bột giảm khoảng 25,26%. Giai đoạn tạo TiC bắt đầu ở nhiệt độ khoảng 1266ºC và kết thúc ở nhiệt độ khoảng 1332oC. Khối lượng bột giảm xuống ở giai đoạn này khoảng 13,16%. Đối với mẫu 6 giờ nghiền tổng khối lượng hỗn hợp bột giảm xuống khoảng 38,42%.
[caption id="attachment_1365" align="aligncenter" width="259"]
Hình 1. Đường cong DTA và TG của mẫu sau 6 giờ nghiền[/caption]
Hình 1 cho thấy, phản ứng tạo thành TiOxCy bắt đầu từ nhiệt độ 1266ºC và hoàn thành trong 6,5 phút khi nung đến nhiệt độ 1332ºC. Trong nghiên cứu về khử nhiệt cacbon tổng hợp TiC [9], Y.-C.Woo cho rằng, phản ứng tạo thành TiOxCy hoàn thành ở nhiệt độ 1500ºC trong 5 phút trong môi trường khí Ar. Như vậy, so với mẫu không nghiền, nhiệt độ phản ứng tạo TiOxCy cũng giảm xuống đối với mẫu có nghiền năng lượng cao.
Đường cong biến đổi khối lượng (TG) trên hình 1 chỉ ra rằng, lượng khí oxit cacbon thoát ra ở cả hai giai đoạn này làm khối lượng bột giảm khoảng 25,26%. Giai đoạn tạo TiC bắt đầu ở nhiệt độ khoảng 1266ºC và kết thúc ở nhiệt độ khoảng 1332oC. Khối lượng bột giảm xuống ở giai đoạn này khoảng 13,16%. Đối với mẫu 6 giờ nghiền tổng khối lượng hỗn hợp bột giảm xuống khoảng 38,42%.
[caption id="attachment_1365" align="aligncenter" width="259"]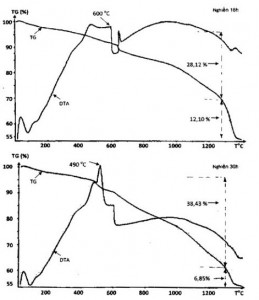 Hình 2. Đường cong DTA và TG các mẫu sau 18 và 30 giờ nghiền[/caption]
Hình 2 là các đường cong phân tích nhiệt của các mẫu nghiền với thời gian tương ứng là 18 và 30 giờ nghiền. Các đường cong DTA cho thấy hỗn hợp bột, đã bắt đầu chuyển biến mạnh ở nhiệt độ 600ºC đối với mẫu nghiền 18 giờ và ở nhiệt độ 490ºC đối với mẫu nghiền 30 giờ. Như vậy, nhiệt độ bắt đầu của quá trình tổng hợp TiC đã giảm mạnh theo thời gian nghiền.
So sánh đường cong DTA của các mẫu với thời gian nghiền khác nhau, thấy rõ nhiệt độ bắt đầu của các giai đoạn chuyển biến giảm xuống khi tăng thời gian nghiền. Lý do là thời gian nghiền tăng làm tăng diện tích bề mặt tiếp xúc giữa các hạt khác chất, tăng mật độ khuyết tật mạng và đồng thời làm giảm kích thước hạt. Do tốc độ phản ứng ở trạng thái rắn phụ thuộc mạnh vào diện tích bề mặt tiếp xúc, cơ chế chủ yếu của các phản ứng ở trạng thái rắn chính là sự khuếch tán. Mật độ khuyết tật mạng tăng, kích thước hạt giảm xuống thúc đẩy quá trình khuếch tán trong mạng tinh thể [11, 12]. Như vậy, sự giảm kích thước hạt, tăng diện tích bề mặt tiếp xúc và mật độ khuyết tật mạng do cơ năng mang lại đã làm quá trình tổng hợp TiC từ TiO2 và C xảy ra ở nhiệt độ thấp hơn.
Đường cong biến đổi khối lượng (TG) của các mẫu nghiền cho thấy khối lượng khí thoát ra của các phản ứng cũng tăng theo thời gian nghiền. Kết thúc giai đoạn tạo tiền chất TiC, khối lượng hỗn hợp bột đã giảm 28,12 % đối với mẫu nghiền 18 giờ và 38,43 % đối với mẫu nghiền 30 giờ. Tổng khối lượng hỗn hợp bột đã giảm xuống trong quá trình tổng hợp TiC là 42,22 % và 45,28 % tương ứng đối với mẫu nghiền 18 và 30 giờ. Tổng khối lượng hỗn hợp bột giảm xuống theo thời gian nghiền chứng tỏ hàm lượng oxy thoát ra trong quá trình thiêu kết tổng hợp TiC đã tăng lên, có nghĩa là hàm lượng oxy trong TiC càng thấp khi thời gian nghiền càng cao.
Hình 2. Đường cong DTA và TG các mẫu sau 18 và 30 giờ nghiền[/caption]
Hình 2 là các đường cong phân tích nhiệt của các mẫu nghiền với thời gian tương ứng là 18 và 30 giờ nghiền. Các đường cong DTA cho thấy hỗn hợp bột, đã bắt đầu chuyển biến mạnh ở nhiệt độ 600ºC đối với mẫu nghiền 18 giờ và ở nhiệt độ 490ºC đối với mẫu nghiền 30 giờ. Như vậy, nhiệt độ bắt đầu của quá trình tổng hợp TiC đã giảm mạnh theo thời gian nghiền.
So sánh đường cong DTA của các mẫu với thời gian nghiền khác nhau, thấy rõ nhiệt độ bắt đầu của các giai đoạn chuyển biến giảm xuống khi tăng thời gian nghiền. Lý do là thời gian nghiền tăng làm tăng diện tích bề mặt tiếp xúc giữa các hạt khác chất, tăng mật độ khuyết tật mạng và đồng thời làm giảm kích thước hạt. Do tốc độ phản ứng ở trạng thái rắn phụ thuộc mạnh vào diện tích bề mặt tiếp xúc, cơ chế chủ yếu của các phản ứng ở trạng thái rắn chính là sự khuếch tán. Mật độ khuyết tật mạng tăng, kích thước hạt giảm xuống thúc đẩy quá trình khuếch tán trong mạng tinh thể [11, 12]. Như vậy, sự giảm kích thước hạt, tăng diện tích bề mặt tiếp xúc và mật độ khuyết tật mạng do cơ năng mang lại đã làm quá trình tổng hợp TiC từ TiO2 và C xảy ra ở nhiệt độ thấp hơn.
Đường cong biến đổi khối lượng (TG) của các mẫu nghiền cho thấy khối lượng khí thoát ra của các phản ứng cũng tăng theo thời gian nghiền. Kết thúc giai đoạn tạo tiền chất TiC, khối lượng hỗn hợp bột đã giảm 28,12 % đối với mẫu nghiền 18 giờ và 38,43 % đối với mẫu nghiền 30 giờ. Tổng khối lượng hỗn hợp bột đã giảm xuống trong quá trình tổng hợp TiC là 42,22 % và 45,28 % tương ứng đối với mẫu nghiền 18 và 30 giờ. Tổng khối lượng hỗn hợp bột giảm xuống theo thời gian nghiền chứng tỏ hàm lượng oxy thoát ra trong quá trình thiêu kết tổng hợp TiC đã tăng lên, có nghĩa là hàm lượng oxy trong TiC càng thấp khi thời gian nghiền càng cao.
| τnghiền (h) | 6 | 12 | 18 | 24 | 30 |
| % Δm giảm sau khi tạo tiền chất | 25,26 | 26,39 | 28,12 | 30,88 | 38,43 |
| % Δm giảm sau khi tạo TiC | 38,42 | 41,92 | 42,22 | 43,44 | 45,28 |
Bảng 1. Sự biến đổi khối lượng bột theo thời gian nghiền
Bảng 1 là kết quả thực nghiệm cho biết sự thay đổi khối lượng hỗn hợp bột trong quá trình thiêu kết tổng hợp TiC từ anataz và muội than, theo thời gian nghiền năng lượng cao. [caption id="attachment_1366" align="aligncenter" width="300"]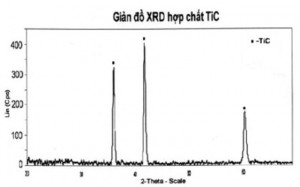 Hình 3. Giản đồ nhiễu xạ rơnghen của mẫu nghiền 18 giờ[/caption]
Hình 3 là giản đồ nhiễu xạ rơnghen của mẫu nghiền 18 giờ sau khi thiêu kết tổng hợp TiC. Phân tích các số liệu thực nghiệm, thấy rằng hợp chất TiC nhận được có hằng số mạng tăng lên khi thời gian nghiền tăng. Cụ thể, đối với các mẫu nghiền 18 và 30 giờ hằng số mạng của hợp chất TiC có giá trị tương ứng là 4,310 và 4,313. Theo Kiparisov [5], hằng số mạng của TiC phụ thuộc vào hàm lượng C liên kết và hàm lượng O chứa trong hợp chất. Giá trị hằng số mạng tăng lên khi %C liên kết tăng lên và %O giảm xuống trong hợp chất. Hằng số mạng của TiC khoảng 4,326 khi nó chứa lượng oxy thấp nhất (%O≈0) [5]. Theo tính toán từ phản ứng (5), hợp chất TiC nhận được khi phản ứng xảy ra hoàn toàn thì lượng khí thoát ra trong hỗn hợp bột là khoảng 48,28 %. So sánh với khối lượng khí thoát ra trong quá trình thiêu kết của mẫu nghiền 30 giờ là 45,28 % và hằng số mạng là 4,313 thì hợp chất TiC nhận được ở đây hoàn toàn chấp nhận được.
Hình 3. Giản đồ nhiễu xạ rơnghen của mẫu nghiền 18 giờ[/caption]
Hình 3 là giản đồ nhiễu xạ rơnghen của mẫu nghiền 18 giờ sau khi thiêu kết tổng hợp TiC. Phân tích các số liệu thực nghiệm, thấy rằng hợp chất TiC nhận được có hằng số mạng tăng lên khi thời gian nghiền tăng. Cụ thể, đối với các mẫu nghiền 18 và 30 giờ hằng số mạng của hợp chất TiC có giá trị tương ứng là 4,310 và 4,313. Theo Kiparisov [5], hằng số mạng của TiC phụ thuộc vào hàm lượng C liên kết và hàm lượng O chứa trong hợp chất. Giá trị hằng số mạng tăng lên khi %C liên kết tăng lên và %O giảm xuống trong hợp chất. Hằng số mạng của TiC khoảng 4,326 khi nó chứa lượng oxy thấp nhất (%O≈0) [5]. Theo tính toán từ phản ứng (5), hợp chất TiC nhận được khi phản ứng xảy ra hoàn toàn thì lượng khí thoát ra trong hỗn hợp bột là khoảng 48,28 %. So sánh với khối lượng khí thoát ra trong quá trình thiêu kết của mẫu nghiền 30 giờ là 45,28 % và hằng số mạng là 4,313 thì hợp chất TiC nhận được ở đây hoàn toàn chấp nhận được.
|
τnghiền (h) |
6 | 12 | 18 | 24 | 30 |
|
a - hằng số mạng (Å) |
4,308 | 4,309 | 4,310 | 4,312 | 4,313 |
Bảng 2. Sự biến đổi hằng số mạng theo thời gian nghiền
Bảng 2 là kết quả xác định sự biến đổi hằng số mạng của hợp chất TiC nhận được theo thời gian nghiền năng lượng cao. 4. Kết luận Kết quả phân tích nhiễu xạ rơnghen và các đường cong TG, DTA của những mẫu nghiền với thời gian khác nhau cho thấy nghiền năng lượng cao ảnh hưởng tới quá trình thiêu kết tổng hợp TiC từ TiOiO2 và C. Trong quá trình này, nhiệt độ bắt đầu khử oxy giảm từ 698ºC xuống 490ºC tương ứng khi thời gian nghiền tăng từ 6 giờ lên 30 giờ. Lượng oxy thoát ra từ hỗn hợp bột tương ứng với khối lượng bột mất đi tăng lên từ 38,42% đến 45,28% khi thời gian nghiền tăng từ 6 giờ lên 30 giờ. Hằng số mạng của TiC phụ thuộc tuyến tính vào hàm lượng C liên kết trong hợp chất. Đại lượng này cũng tăng lên từ 4,308 đến 4,313 khi thời gian nghiền tăng từ 6 giờ lên 30 giờ. Tài Liệu Trích Dẫn- Trần Quốc Lập, Vũ Huy Thăng, Vũ Lai Hoàng; ảnh hưởng của năng lượng cơ học đến nhiệt độ tổng hợp TiCiC từ TiO2 và muội than, Tạp chí Khoa học và Công nghệ Kim loại, số 29, 2010, tr. 45-49
- Г. В. Самсонов, Тугоплавкие соединения, Государственное научно-техническое издателъство, Москва, 1963
- P. Kиффep, П. Швapцкoпф; Твepдыe cплaвы, Мeтaллypгиздaт, 1957
- Г. П. Лyчинсий, Химия титана, Химия, 1971
- С. С. Кипарисов, Ю. В. Левинский, Карбид титана, Металлургия, Москва, 1987
- L.-M. Berger, P. Ettmayer and B. Schultrich; Influencing factors on the carbothermal reduction of titanium dioxide without and with simultaneous nitridation, Int. J. of refractory metals and hard materials, 12, 1993- 1994, p. 161-172
- M. Razavi, M. R. Rahimipour, R. Kaboli; Synthesis of TiC nanocomposite powder from impure TiO2 and car- bon black by mechanically activated sintering, Journal of alloys and compounds, 460, 2008, p. 694-698
- L.-M. Berger, W. Gruner, E. Langholf, S. Stolle; On the mechanism of carbothermal reduction processes of TiO2 and ZrO2, International Journal of Refractory Metals and Hard Materials, 17, 1999, p. 235-243
- Young-Chul Woo, Ho-Jae Kang, Deug J. Kim; Formation of TiC particle during carbothermal reduction of TiO2, Journal of the European Ceramic Society, 27, 2007, p. 719-722
- L. Lu, M. O. Lai, S. Zhang; Diffusion in mechanical alloying, Journal of Materials Processing Technology, 67, 1997, p. 100-104
- C. Suryanarayana, Mechanical alloying and milling, Progress in Materials Science, 46, 2001, p. 1-184
- 12. V. N. Likhachev, G. A. Vinogradov, M. I. Alymov; Anomalous heat capacity of nanoparticles, Physics Letters, A357, 2006, p. 236-239







